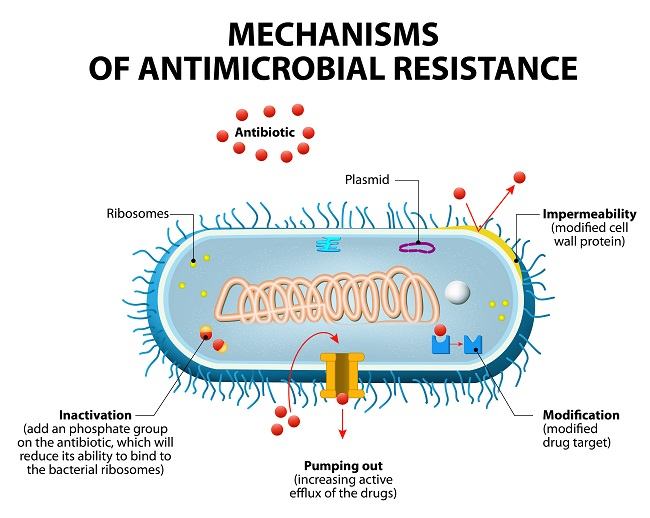
Meningkatnya infeksi bakteri gram negatif resisten karbapenem menjadi momok bagi kesehatan masyarakat. Hal ini disebabkan oleh ditemukannya patogen resisten karbapenem dan kurangnya opsi terapi yang efektif dan aman.
Salah satu dari masalah tersebut adalah infeksi bakteri gram negatif resisten karbapenem yang meliputi infeksi patogen Enterobacteriaceae spp., Pseudomonas aeruginosa, Acinetobacter baumannii dan Stenotrophomonas maltophilia. Ancaman nyata dari infeksi bakteri gram negatif resisten karbapenem dilandasi oleh adanya peningkatan insidens di seluruh dunia, resistensi dan keterbatasan pilihan antibiotik yang ada, serta angka mortalitas yang tinggi.[1-3]
Colistin, tigecycline, dan minocycline telah digunakan sebagai agen lini pertama untuk terapi infeksi bakteri gram negatif resisten karbapenem tapi efikasinya masih kurang memuaskan dan data percobaan klinisnya pun masih terbatas.[4-7]
Namun, perjuangan mencari solusi terhadap permasalahan tersebut tampaknya mulai membuahkan hasil. Saat ini sudah tersedia sejumlah antibiotik baru yang telah melengkapi penelitian klinis tahap akhir untuk penatalaksanaan infeksi bakteri gram negatif resisten karbapenem yaitu ceftazidime-avibactam, ceftolozane-tazobactam, meropenem-vaborbactam, plazomicin, eravasiklin, imipenem-cilastatin-relebactam, dan cefiderocol.[8,9]
Ceftazidime-Avibactam
Avibactam merupakan diazabicyclooctane beta-lactamase inhibitor (BLI) yang diberikan dengan kombinasi ceftazidime sudah diakui secara resmi untuk penatalaksanaan kasus infeksi intra abdomen dengan komplikasi/complicated intra abdominal infection (cIAI) , infeksi saluran kemih dengan komplikasi/complicated urinary tract infection (cUTI) maupun penatalaksanaan pneumonia komunitas maupun hospital-acquired bacterial pneumonia (HABP) dan ventilator-associated bacterial pneumonia (VABP).
Kombinasi ceftazidime-avibactam aktif terhadap carbapenemases (KPC)-producing carbapenem-resistant Enterobacteriaceae (CRE) termasuk karbapenemase kelas A dan D namun tidak untuk karbapenemase kelas B seperti New Delhi metallo beta lactamase (NDM). Mayoritas strain karbapenem resisten P. aeruginosa rentan terhadap ceftazidime-avibactam. Kombinasi ceftazidime-avibactam tidak aktif terhadap Acinetobacter baumannii atau Stenotrophomonas maltophilia.[8]
Sejumlah data penelitian klinis fase 3 menyokong efikasi penggunaan kombinasi ceftazidime-avibactam untuk kasus infeksi gram negatif resisten karbapenem. Studi Ceftazidime-Avibactam Compared With Doripenem Followed by Oral Therapy for Hospitalized Adults With Complicated Urinary Tract Infection (RECAPTURE) merekrut 1033 pasien yang diberikan ceftazidime-avibactam atau doripenem secara acak.
Hasil analisis menemukan bahwa combined symptomatic resolution/microbiological eradication at test of cure (TOC) 71,2% vs 64,5% untuk keunggulan ceftazidime-avibactam. Pada penelitian lainnya oleh Mazuski et al, sebanyak 1066 pasien dengan cIAI mendapat ceftazidime-avibactam plus metronidazole atau meropenem.
Clinical cure rate pada TOC untuk kombinasi ceftazidime-avibactam plus metronidazole sebanding atau non inferior terhadap meropenem (81,6% vs 85,1%). Hasil serupa ditemukan pada studi fase 3 REPRISE yang melibatkan 333 pasien dengan cUTI atau cIAI yang disebabkan oleh ceftazidime resisten Enterobacteriaceae atau strain P. aeruginosa.
Selain itu, studi Comparing Ceftazidime-Avibactam Versus Meropenem in Hospitalized Adults with Nasocomial Pneumonia (REPROVE) merekrut 879 pasien yang diberikan ceftazidime-avibactam atau meropenem secara acak. Populasi sampel didominasi oleh patogen K. pneumoniae (37%) dan P. aeruginosa (30%) dan 28% diantaranya tidak rentan terhadap ceftazidime. Pada analisis populasi modified intention-to-treat (mITT), sebanyak 68,8% di grup ceftazidime-avibactam sembuh secara klinis vs 73% di grup meropenem.[8]
Ceftolozane-Tazobactam
Ceftolozane merupakan sefalosporin 3’-aminopyrazolium yang baru dengan aktivitas luas terhadap strain P.aeruginosa. Kombinasinya dengan tazobactam semakin memperkuat aktivitas antipseudomonas sekaligus memperluas aktivitas terhadap strain bakteri yang menghasilkan extended-spectrum beta laktamase (ESBL).
Kombinasi ceftolozane-tazobactam aktif terhadap carbapenem-nonsusceptible P. aeruginosa tapi tidak aktif terhadap CRE Acinetobacter baumannii atau Stenotrophomonas maltophilia.[8]
Studi Non Inferioritas pada Ceftolozane-Tazobactam
Penelitian Comparing the Safety and Efficacy of Intravenous CXA-201 and Intravenous Levofloxacin in Complicated Urinary Tract Infection, Including Pyelonephritis (ASPECT-cUTI) melibatkan 1083 pasien dengan cUTI termasuk pielonefritis akut mendapatkan ceftolozane-tazobactam atau levofloxacin. Hasil studi menemukan bahwa composite cure rate sebesar 76,9% vs 68,4% pada populasi mITT untuk keunggulan ceftolozane-tazobactam.
Sedangkan studi Comparing the Safety and Efficacy of Intravenous CXA-201 and Intravenous Meropenem in Complicated Intraabdominal Infections (ASPECT-cIAI) yang melibatkan 993 pasien cIAI yang mendapatkan ceftolozane-tazobactam atau meropenem menemukan bahwa clinical cure rate pada TOC di populasi mITT sebesar 83% vs 87,3% (sebanding).
Kedua studi tersebut memenuhi kriteria margin non inferioritas. Selain itu, hasil studi fase 3 Safety and Efficacy Study of Ceftolozane-Tazobactam to Treat Ventilated Nosocomial Pneumonia (ASPECT-NP) menemukan hasil sebanding untuk all-cause-mortality pada hari ke-28 maupun untuk clinical cure rate antara ceftolozane-tazobactam dengan meropenem.
Namun, data klinis untuk strain Pseudomonas aeruginosa masih terbatas. Pada sebuah data serial 21 pasien dengan infeksi Pseudomonas aeruginosa resisten karbapenem, 71% (15/21) sembuh secara klinis dan 30-day all-cause mortality hanya 10% pada penggunaan ceftolozane-tazobactam.[8]
Meropenem-Vaborbactam
Vaborbactam merupakan BLI boronic acid pertama yang diketahui mampu menginhibisi secara reversibel kompetitif terhadap serine-beta laktamase. Vaborbactam menginhibisi beta laktamase kelas A termasuk KPC karbapenemase, namun tidak aktif terhadap kelas B seperti NDM karbapenemase dan verona integron-encoded metallo-β-lactamase (VIM) karbapenemase dan kelas D beta laktamase.
Vaborbactam juga menginhibisi kelas A ESBL dan kelas C AmpC beta laktamase. Vaborbactam dikembangkan bersama dengan kombinasi meropenem karena konsistensi farmakokinetik kedua agen tersebut.[8]
Studi fase 3 Efficacy/Safety of Meropenem-Vaborbactam Compared to Piperacillin-Tazobactam in Adults With cUTI and Acute Pyelonephritis (TANGO-I) melibatkan 550 pasien cUTI/AP untuk diberikan meropenem-vaborbactam atau piperacillin-tazobactam secara acak.
Endpoint primer untuk composite clinical and microbiological cure pada populasi mMITT tercapai pada 98,4% grup meropenem-vaborbactam vs 94% pada grup piperacillin-tazobactam. Sedangkan studi Efficacy, Safety, Tolerability of Vabomere Compared to Best Available Therapy in Treating Serious Infections in Adults (TANGO-II) pada 72 pasien dengan cUTI, HABP/VABP, cIAI yang disebabkan oleh patogen CRE menemukan keunggulan efikasi meropenem-vaborbactam.[8]
Plazomicin
Plazomicin merupakan derivat sintetis sisomicin yang termasuk golongan aminoglikosida. Plazomicin aktif terhadap famili Enterobacteriaceae termasuk strain yang resisten terhadap aminoglikosida saat ini seperti amikacin, gentamicin, tobramycin. Aktivitas plazomicin terhadap Pseudomonas aeruginosa dan Acinetobacter baumannii secara umum sebanding dengan aminoglikosida lainnya.[8]
Dua penelitian fase 3 terhadap plazomicin sudah lengkap. Penelitian pertama yaitu studi A Study of Plazomicin Compared With Meropenem for the Treatment of Complicated Urinary Tract Infection /cUTI Including Acute Pyelonephritis (EPIC) melibatkan 609 pasien cUTI termasuk pielonefritis akut.
Composite clinical dan microbiological cure rates pada populasi mITT sebesar 88% untuk plazomicin vs 91,4% untuk meropenem pada hari ke-5 dan 81,7%-plazomicin vs 70,1%-meropenem pada TOC. Namun dilaporkan ada peningkatan serum kreatinin yang lebih besar pada grup plazomicin jika dibandingkan dengan meropenem (7% vs 4%).
Penelitian kedua difokuskan pada infeksi bloodstream, HABP/VABP yang disebabkan oleh A Study of Plazomicin Compared With Colistin in Patients With Infection Due to Carbapenem-Resistant Enterobacteriaceae (CRE/CARE). Diantara 39 pasien yang dievaluasi, rate of 28 day all-cause mortality lebih rendah pada grup plazomicin daripada grup colistin (11,8% vs 40%) dengan benefit survival amat signifikan pada infeksi bloodstream (7,1% vs 40%). Insiden peningkatan serum kreatinin lebih rendah pada plazomicin jika dibandingkan dengan colistin (16,7% vs 50%).[8]
Eravasiklin
Eravasiklin merupakan sintetik tetrasiklin. Eravasiklin aktif terhadap patogen gram negatif termasuk CRE, strain resisten karbapenem Acinetobacter baumannii dan Stenotrophomonas maltophilia tetapi tidak aktif terhadap Pseudomonas aeruginosa. Eravasiklin juga aktif terhadap methicillin-resistant S.aureus dan vancomycin-resistant enterococci.[8]
Hasil Studi IGNITE 1
Sudah ada tiga penelitian klinis fase 3 terhadap eravasiklin. Pada studi Efficacy and Safety Study of Eravacycline Compared With Ertapenem in Complicated Intra-abdominal Infections (IGNITE 1) yang melibatkan 541 pasien yang diberikan eravasiklin atau ertapenem menemukan clinical cure rate pada TOC sebesar 86,8% pada grup eravasiklin vs 87,6% pada grup ertapenem.
Hasil Studi IGNITE 2
Sedangkan pada studi Efficacy and Safety Study of Eravacycline Compared With Levofloxacin in Complicated Urinary Tract Infections (IGNITE 2) melibatkan 908 pasien yang diberikan eravasiklin atau levofloxacin, namun margin noninferioritas -10% tidak terpenuhi.
Hasil Studi IGNITE 3
Hasil ini ditindaklanjuti oleh pihak pembuat eravasiklin dengan melakukan studi Efficacy and Safety Study of Eravacycline Compared With Ertapenem in Participants With Complicated Urinary Tract Infections (IGNITE 3) dan Efficacy and Safety Study of Eravacycline Compared With Meropenem in Complicated Intra-abdominal Infections (IGNITE 4). Hasil studi IGNITE 3 menemukan bahwa composite clinical and microbiological success rate untuk eravasiklin 68,5% vs 74,9% pada saat TOC, namun tetap tidak memenuhi kriteria margin non inferioritas -10% (unpublished data).
Hasil Studi IGNITE 4
Sedangkan hasil studi IGNITE 4 menemukan hasil clinical cure rate 90,8% pada grup eravasiklin vs 91,2% pada grup meropenem untuk keunggulan eravasiklin pada kasus cIAI. Berdasarkan hasil tersebut Food and Drug Administration baru mengesahkan eravasiklin untuk terapi cIAI pada tahun 2018.[8]
Imipenem-Cilastatin-Relebactam
Relebactam merupakan BLI baru dengan inti diazabicyclooctane serupa dengan avibactam. Relebactam menginhibisi beta laktamase kelas A termasuk KPC karbapenemase dan beta laktamase kelas C. Relebactam secara substansial memulihkan aktivitas imipenem-cilastatin terhadap mayoritas strain penghasil KPC, dan strain resisten karbapenem Pseudomonas aeruginosa namun tidak aktif terhadap Acinetobacter baumannii atau Stenotrophomonas maltophilia.[8]
Ada dua studi fase 2 yang memperlihatkan efikasi dan keamanan penggunaan kombinasi imipenem-cilastatin-relebactam. Studi pertama merekrut 302 pasien cUTI/AP untuk mendapatkan imipenem-cilastatin atau imipenem-cilastatin plus relebactam. Rates of microbiological response pada akhir terapi pada populasi microbiologically evaluable (ME) sebanding antara kedua jenis terapi.
Sedangkan studi kedua tetap menggunakan kedua jenis terapi namun diterapkan pada 351 pasien cIAI. Clinical response pada akhir terapi di populasi ME berada pada kisaran 95,2 hingga 98,8% pasien. Regimen imipenem-cilastatin dengan relebactam dapat ditolerir dengan baik seperti regimen imipenem-cilastatin tanpa relebactam.
Perbandingan Regimen Imipenem-Cilastatin-Relabactam dengan Regimen Lain
Pada penelitian lanjutan, studi Efficacy and Safety of Imipenem-Cilastatin/Relebactam VS Colistimethate Sodium-Imipenem-Cilastatin in Imipenem- Resistant Bacterial Infection fase 3 (RESTORE-IMI 1) pada pasien VABP, HABP, cIAI dan cUTI yang disebabkan oleh bakteri gram negatif resisten imipenem menemukan bahwa clinical response pada regimen imipenem-cilastatin-relabactam lebih baik daripada regimen imipenem-cilastatin-colistin (71,4% vs 40%) dan 29-day-all-cause-mortality lebih rendah pada grup imipenem-cilastatin-relebactam. Selain itu, kejadian efek merugikan terkait obat lebih rendah pada grup imipenem-cilastatin-relabactam.[8]
Cefiderocol
Cefiderocol merupakan siderophore cephalosporin dimana rantai samping katekol membentuk chelated complex dengan ferric iron. Hal ini memungkinkan cefiderocol untuk secara aktif melewati membran luar bakteri gram negatif masuk ke ruang periplasma.
Cefiderocol stabil terhadap hidrolisis dari beta laktamase kelas A (termasuk KPC, ESBL), kelas B (termasuk NDM,VIM, IMP, L1), kelas C (AmpC) maupun kelas D (termasuk OXA-48 Enterobacteriaceae dan OXA-23, OXA-24 Acinetobacter baumannii). Oleh sebab itu, cefiderocol aktif terhadap semua bakteri gram negatif mulai dari Enterobacteriaceae, Pseudomonas aeruginosa, Acinetobacter baumannii, dan Stenotrophomonas maltophilia termasuk strain resisten karbapenem.[8,9]
Studi fase 2 A Study of Efficacy and Safety of Intravenous Cefiderocol (S-649266) Versus Imipenem/Cilastatin in Complicated Urinary Tract Infections (APEKS-cUTI) melibatkan 452 pasien cUTI untuk mendapatkan cefiderocol atau imipenem-cilastatin. Composite clinical and microbiological efficacy endpoint at TOC terpenuhi pada 72,6% vs 54,6% untuk keunggulan cefiderocol. Studi tersebut memenuhi kriteria non inferioritas -15%.
Saat ini masih berlangsung penelitian A MultiCenter, RandomizED, Open-label ClInical Study of S-649266 or Best AvailabLE Therapy for the Treatment of Severe InfectionsCaused by Carbapenem-Resistant Gram-negative Pathogens (CREDIBLE-CR) dan A Multicenter, Randomized, Double-blind, Parallel-group, Clinical Study of S-649266 Compared With Meropenem for the Treatment of Hospital Acquired Bacterial Pneumonia, Ventilator-associated Bacterial Pneumonia, or Healthcare-associated Bacterial Pneumonia Caused by Gram-negative Pathogens (APEKS-NP).[8]
Kesimpulan
Meski membutuhkan waktu yang lama, data positif penelitian klinis fase akhir dari ceftazidime-avibactam, ceftolozane-tazobactam, meropenem-vaborbactam, plazomicin, eravasiklin, imipenem-cilastatin-relebactam, dan cefiderocol memberi harapan baru untuk solusi pilihan antibiotik terhadap masalah infeksi bakteri gram negatif resisten karbapenem.
Pencegahan menjadi salah satu upaya untuk menurunkan resistensi antibiotik. Pemberian antibiotik dengan tepat dan rasional serta mengurangi healthcare-associated infection dengan cara mencuci tangan sesuai dengan five-moments, melakukan tindakan medis dengan indikasi yang sesuai, menggunakan stetoskop individual per ranjang pasien, dan penggunaan alat pelindung diri.
Direvisi oleh: dr. Gabriela Widjaja